Pasaulyje gimdos kaklelio vėžys užima 4 vietą tarp naujai diagnozuotų moterų vėžio atvejų ir sudaro beveik 8 proc. visų vėžio atvejų [1]. Nuo 2006 metų Lietuvoje pastebima sergamumo gimdos kaklelio vėžiu mažėjimo tendencija: 2006 metais užregistruoti 541 nauji gimdos kaklelio vėžio atvejai, 2007 metais – 487, 2008 metais – 524, 2009 metais – 457, 2010 metais – 506, 2011 metais – 452 ir 2012 metais – 431 atvejis. Žmogaus papilomos virusas (ŽPV) yra pagrindinis gimdos kaklelio neoplazijos išsivystymo rizikos veiksnys ir gali būti nustatytas 99,7 proc. moterų, sergančių gimdos kaklelio vėžiu [2]. Sergant invaziniu gimdos kaklelio vėžiu, dažniausiai nustatomi ŽPV 16 ir / ar 18 tipai, kurie sudaro iki 71 proc. visų atvejų [3]. Nors pasaulyje, kaip ir Lietuvoje, taikomos prevencinės gimdos kaklelio vėžio programos, gimdos kaklelio vėžys vis dar dažniausiai diagnozuojamas vėlyvųjų stadijų. 5 metų išgyvenamumas sergant I stadijos gimdos kaklelio karcinoma siekia 80–93 proc., o sergant III stadijos gimdos kaklelio karcinoma – tik 32–35 proc., IV stadijos – apie 15 proc. [4].
Nors ligos priežastiniai veiksniai daugeliu atvejų yra aiškūs, tačiau didelis sergamumas ir vėlyva diagnostika vis dar išlieka pagrindine problema, o mažas gydymo galimybių pasirinkimas, nedidelės sisteminio gydymo galimybės kelia naujų, inovatyvių, gerokai išgyvenimo trukmę prailginančių gydymo metodų būtinybės klausimą.
Literatūros apžvalga
Šiuo metu pasaulyje vietiškai išplitusio ir progresuojančio neoperabilaus gimdos kaklelio vėžio naujausias gydymo metodas yra chemoterapija, derinama su biologine terapija bevacizumabu, angiogenezės inhibitoriumi. Bevacizumabas – rekombinantinis humanizuotas monokloninis antikūnas, kuris slopina naviko angiogenezę, inhibuodamas kraujagyslių endotelio augimo faktorių A (VEGF-A) [5]. Naviko ląstelės ekspresuoja VEGF, kuris skatina naviko vaskuliarizaciją, taip aprūpindamas vėžines ląsteles mitybinėmis medžiagomis ir deguonimi. Bevacizumabas, veikdamas per VEGF blokavimą, skatina naviko ląstelių žūtį ir mažina ligos metastazavimo riziką [6].
Chemoterapija platinos pagrindu, derinama su bevacizumabu, pasaulyje yra pirmojo pasirinkimo gydymo metodas esant recidyvavusiam, metastazavusiam ar progresuojančiam neoperabiliam gimdos kaklelio vėžiui [7]. Šios gydymo rekomendacijos pagrįstos Gynecologic Oncology Group 240 (GOG 240) klinikinio tyrimo duomenimis. Tyrimo duomenimis, bendrasis išgyvenamumas (BI) naudojant chemoterapiją platinos pagrindu, derinamą su bevacizumabu, buvo 16,8 mėnesio, palyginti su 13,3 mėnesio BI pacienčių, gavusių tik chemoterapiją. Moterų, kurioms anksčiau nebuvo taikyta dubens organų radioterapija, BI taikant sisteminį gydymą siekė 24,5 mėnesio, palyginti su 16,8 mėnesio moterų, gavusių tik chemoterapiją. Palyginus išgyvenamumą moterų, gavusių chemoterapiją su bevacizumabu ir gavusių tik chemoterapiją po diagnozuoto ligos progresavimo, didesnių išgyvenamumo skirtumų nebuvo (8,4 mėnesio, palyginti su 7,1 mėnesio). Ligos atsakas į gydymą nustatytas net 49 proc. pacienčių, palyginti su 36 proc. sergančių moterų, gavusių tik chemoterapiją [8–9].
Kaip ir kiekvienas sudėtinis gydymas, chemoterapija, derinama su biologine terapija, sukelia daugiau nepageidaujamų reiškinių. Klinikinio tyrimo duomenimis, dažniausiai pasireiškė arterinio kraujo spaudimo svyravimas ar anksčiau diagnozuotos arterinės hipertenzijos pablogėjimas (iki 25 proc. pacienčių). Kiti dažnesni kliniškai reikšmingi nepageidaujami reiškiniai, tokie kaip genitointestinalinė fistulė (apie 3 proc.), genitourinarinė fistulė (apie 3 proc.), III–IV laipsnio neutropenija (apie 36 proc., palyginti su 26 proc. tarp gavusių tik chemoterapiją) ir arterioveninė trombozė ar tromboembolija (apie 8 proc.), sutrikęs žaizdų gijimas bei izoliuota proteinurija, pasireiškė rečiau ir buvo labiau susiję su biologinės terapijos nepageidaujamu poveikiu [7–10]. Per pirmuosius 9 gydymo mėnesius nebuvo didesnių gyvenimo kokybės skirtumų tarp ligonių, gavusių chemoterapiją su biologine terapija, ir ligonių, gavusių tik chemoterapiją [9, 10].
Taigi, remiantis GOG 204 tyrimu, bevacizumabas, derinamas su chemoterapija platinos pagrindu, nuo 2014 metų yra patvirtintas kaip efektyviausias pirmojo pasirinkimo metodas, taikomas recidyvavusiam, progresuojančiam ar metastazavusiam gimdos kaklelio vėžiui gydyti. Šis gydymo metodas nuo 2016 metų yra sėkmingai taikomas Lietuvoje, taip pat ir Nacionaliniame vėžio institute (NVI). Šiame straipsnyje apžvelgsime gimdos kaklelio vėžio gydymo bevacizumabu NVI statistiką.
NVI patirtis gydant gimdos kaklelio vėžį angiogenezės inhibitoriumi
Ligonių ir ligos charakteristikos
Vietiškai išplitusios, neoperabilios, metastazavusios ar progresuojančios gimdos kaklelio karcinomos chemoterapija, derinama su bevacizumabu, pagal šiuo metu Lietuvos Respublikoje galiojančią vaistų kompensavimo tvarką, NVI yra skiriama nuo 2016 metų liepos mėnesio. Per šį laikotarpį NVI buvo diagnozuotas 261 naujas gimdos kaklelio karcinomos atvejis. Net 46 moterims jau diagnozės pradžioje buvo patvirtinta IV ligos stadija. 18 iš šių pacienčių (39 proc.) kaip pirminis gydymas buvo taikomas chemospindulinis gydymas, 3 (7 proc.) – tik spindulinis gydymas, 12 pacienčių (26 proc.) būklė diagnozės pradžioje buvo per sunki chemoterapiniam gydymui. Nuo to laiko iki 2018 metų rugpjūčio mėnesio bevacizumabu, derinamu su chemoterapija (schema – cisplatina / paklitakselis), buvo gydomos 32 gimdos kaklelio karcinoma sergančios moterys. 13 jų (40 proc.) gydymas buvo taikomas dėl IV stadijos ligos, likusioms pacientėms (po 6 proc. pirminė diagnozė buvo IB ir IIA stadijos liga, 13 proc. – IIB stadija, 35 proc. – IIIB stadija) gydymas buvo taikomas dėl ligos atkryčio. Amžiaus vidurkis, kai buvo diagnozuotas gimdos kaklelio vėžys, buvo 53 metai. Nustatant diagnozę, jauniausia gydoma pacientė buvo 36 metų, vyriausia – 70 metų. Kaip ir pasaulyje, didžiąją dalį diagnozuotų gimdos kaklelio onkologinių ligų (88 proc.) sudarė plokščialąstelinė karcinoma, likusioji dalis (22 proc.) – adenokarcinoma. Net 88 proc. visų histologinių variantų buvo blogos diferenciacijos (G3) karcinoma. 34 proc. visų ligonių sisteminis gydymas pagal schemą cisplatina / paklitakselis / bevacizumabas buvo taikomas kaip pirmojo pasirinkimo gydymas, tačiau dauguma gydytų moterų jį gavo po nustatyto tolesnio ligos progresavimo (63 proc.) ar esant persistuojančiai ligai po taikyto gydymo (3 proc.). Šioms moterims anksčiau buvo taikytas kitas radikalusis pirminis gydymas: operacinis (3 proc.), chemospindulinis (56 proc.) ar tik spindulinis (9 proc.).
Gydymo ypatumai
Gydymo pagal schemą cisplatina / paklitakselis / bevacizumabas kas 3 savaites ciklų skaičiaus vidurkis siekė 7,65 ciklo. Daugiausia buvo realizuota 13 ciklų, mažiausiai – 2. Nėra didesnio duomenų skirtumo, palyginti NVI turimus duomenis su GOG 240 klinikinio tyrimo duomenimis. Pastarajame vidutinis gydymo ciklų skaičius buvo 6 ciklai, o gydymo ciklų skaičius tarp visų gydytų moterų svyravo nuo 2 iki 12 ciklų [8–10].
Nepageidaujami gydymo reiškiniai
Remiantis GOG 204 tyrimo duomenimis, dažniausi nepageidaujami reiškiniai buvo susiję su biologinės terapijos veikimu. Panaši nepageidaujamo gydymo poveikio tendencija pasireiškė ir tarp NVI gydytų pacienčių. 34 proc. gydytų moterų paūmėjo, tapo sunkai kontroliuojama ar buvo naujai diagnozuota pirminė arterinė hipertenzija, 13 proc. buvo nustatyta izoliuota proteinurija, net 9 proc. gydytų moterų buvo diagnozuotos genitointestinalinės ar genitourinarinės fistulės. Kiti nepageidaujami gydymo reiškiniai (polineuropatija – 44 proc., kaulų skausmai – 28 proc., hematologinis toksiškumas – 13 proc.) gali būti labiau siejami su chemoterapijos poveikiu.
Iš visų gydytų pacienčių gydymas bevacizumabu buvo nutrauktas tik 2 moterims (6 proc.); priežastys – gydant diagnozuotos fistulės. Anksčiau skirtas chemospindulinis gydymas visuomet yra rizikos veiksnys gastrointestinalinio trakto (GI) perforacijai ir fistulių susidarymui. GOG 204 tyrime visoms pacientėms, kurioms išsivystė GI trakto perforacja ar fistulės, anksčiau buvo taikytas chemospindulinis gydymas [9–10]. Chemospindulinis gydymas, kaip pirmojo pasirinkimo gydymas esant ankstyvajai ligos stadijai, buvo taikytas ir NVI gydytoms pacientėms, kurioms gydymo metu buvo diagnozuotos GI trakto fistulės. GI trakto perforacija ir fistulės dažniau diagnozuojamos, jei liga recidyvuoja dubenyje, yra diagnozuota pilvaplėvės karcinozė, anksčiau buvo taikyta spindulinė terapija, yra GI trakto obstrukcija, pakartotinės chirurginės intervencijos, uždegiminės žarnyno ligos ar žarnų rezekcija praeityje.
Gydymo rezultatai
Pradėtas gydymas bevacizumabu iki šiol yra tęsiamas 12 pacienčių (38 proc.). Net 11 pacienčių (34 proc.) šiuo metu yra aktyviai stebimos po baigto gydymo, 2 pacientėms (6 proc.) yra taikomas antrosios eilės paliatyvusis, o 1 pacientei (3 proc.) – simptominis gydymas. Pagrindinės gydymo nutraukimo priežastys buvo progresuojančios ir gyvenimo kokybę bloginančios nepageidaujamos reakcijos (pvz., polineuropatija, 34 proc.), asmeninės pacienčių priežastys (nebeatvyko ar atsisakė tęsti gydymą, 16 proc.), visiškas ligos atsakas (9 proc.) bei tolesnis ligos progresavimas vykstant gydymui (3 proc.). Vidutinis laikas iki ligos progresavimo baigus gydymą buvo 5 mėnesiai (mažiausias – progresavimas vykstant gydymui, ilgiausias laiko tarpas – 11 mėnesių). 4 iš gydytų pacienčių jau yra mirusios, tačiau šios mirtys nesiejamos su gydymo ciplatina / paklitakseliu / bevacizumabu toksiškumu.
Išvados
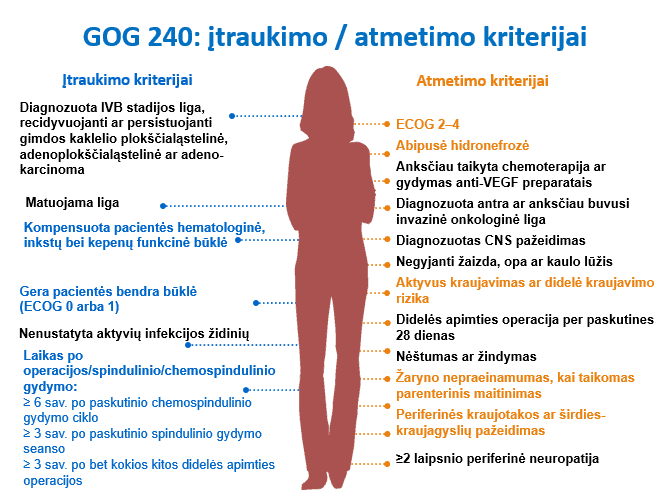
Remdamiesi literatūros, klinikinių tyrimų ir NVI gydytų pacienčių duomenų apžvalga, galime teigti, kad chemoterapija, derinama su biologine terapija bevacizumabu, gerokai prailgina pacienčių, sergančių išplitusiu gimdo kaklelio vėžiu, išgyvenamumą ir teikia daug vilties. Atsižvelgiant į galimus gyvybei pavojingus nepageidaujamus reiškinius, labai svarbu tinkamai atrinkti pacientes gydymui. GOG 240 tyrime buvo naudoti tam tikri griežti atrankos kriterijai, kurie padėjo sumažinti nepageidaujamų reiškinių riziką ir leido tikėtis geresnių gydymo rezultatų (1 pav.) [8–10]. Manome, kad šie kriterijai būtų naudingi gydytojui praktikui prieš apsisprendžiant dėl gydymo angiogenezės inhibitoriumi. Ligonės, kurių bendra būklė pagal ECOG yra 2 ir daugiau, neturėtų būti gydomos bevacizumabu. Diagnozavus abipusę hidronefrozę, prieš pradedant gydymą būtina atkurti šlapimtakių praeinamumą stentavimu arba sumažinti hidronefrozę perkutaniniu inkstų drenavimu. Siekiant sumažinti nepageidaujamų reiškinių riziką, gimdos kaklelio vėžiu sergančioms ligonėms po tam tikrų procedūrų bevacizumabo turėtų būti skiriama tik šiais atvejais:
- praėjus mažiausiai 6 savaitėms po buvusios fistulės, GI trakto perforacijos arba pilvo ertmės absceso drenavimo / operacijos ar spontaninio užgijimo;
- praėjus mažiausiai 6 savaitėms po paskutinio chemospindulinio gydymo kurso;
- praėjus mažiausiai 3 savaitėms po paskutinio radioterapijos seanso.
Gyd. Giedrė Anglickienė1, V. Vaitekėnaitė2, dr. Lina Daukantienė1, doc. dr. Birutė Brasiūnienė1,2
1 Nacionalinio vėžio instituto Chemoterapijos skyrius
2 Vilniaus universiteto Medicinos fakultetas
LITERATŪRA
1. Worldwide data | World Cancer Research Fund International. https://www.wcrf.org/int/cancer-facts-figures/worldwide-data.
2. M Frumovitz. Invasive cervical cancer: Epidemiology, risk factors, clinical manifestations, and diagnosis. UpToDate, 2017 Feb 09.
3. S de Sanjose, et al. Human papillomavirus genotype attribution in invasive cervical cancer: a retrospective cross-sectional worldwide study. Lancet Oncol., 2010 Nov, p. 1048–1056, lapkr. 2010;
4. Survival rates for cervical cancer, by stage. https://www.cancer.org/cancer/cervical-cancer/detection-diagnosis-staging/survival.html.
5. T Shih, C Lindley. Bevacizumab: an angiogenesis inhibitor for the treatment of solid malignancies. Clin. Ther., 2006 nov, p. 1779–1802.
6. HL Goel, AM. Mercurio. VEGF targets the tumour cell. Nat Rev Cancer, 2013 Dec, p. 871–882;
7. JD Wright. Management of recurrent or metastatic cervical cancer. UpToDate, 2018 Jun 26.
8. KS Tewari, et al. Improved survival with bevacizumab in advanced cervical cancer. N. Engl. J. Med., 2014 Feb, p. 734–743.
9. KS Tewari, et al. Bevacizumab for advanced cervical cancer: final overall survival and adverse event analysis of a randomised, controlled, open-label, phase 3 trial (Gynecologic Oncology Group 240). Lancet Lond. Engl., 2017 Oct, p. 1654–1663.
10. RT Penson, et al. Bevacizumab for advanced cervical cancer: patient-reported outcomes of a randomised, phase 3 trial (NRG Oncology-Gynecologic Oncology Group protocol 240). Lancet Oncol., 2015 Mar, p. 301–311.