
DNR pasas yra personalizuotos medicinos, kuri yra šiuolaikinės diagnostikos, gydymo ir prevencijos esmė, pagrindas. Tai galimybė pereiti prie biologiškai suasmenintos medicinos, kurią suteikė iššifruota individualaus žmogaus bei ištisų tautų DNR. Žmogaus DNR analizė lėmė šiuolaikinės diagnostikos, prevencijos ir net vaistų atsiradimą remiantis asmeniniais kiekvieno žmogaus duomenimis, įrašytais genuose. Personalizuota medicina turi nenuginčijamų privalumų – ji leidžia greičiau, tiksliau diagnozuoti, taikyti tik asmeniui pritaikytus gydymo būdus bei tiksliai atskleisti vaiko sveikatos būklę dar iki gimstant.
DNR paso pagrindas yra biologiniai žmonių skirtumai, kuriuos lemia genai. Šiuos genų skirtumus, gautus iš motinos ir tėvo vaisiaus atsiradimo metu, lemia žmogaus geno raktas, kurį žmogaus genomo projekto dėka mokslininkai jau iššifravo. Žmogaus genomo projektas – tai projektas, kuris padėjo iššifruoti žmogaus chromosomų rinkinyje esančių DNR seką, kuri susideda iš trijų milijardų nukleotidų porų. Šiuolaikiniai naujomis genotechnologijomis paremti tyrimai padeda nustatyti visą žmogaus DNR seką. Nuskaičius visą žmogaus genomą ir išsiaiškinus, kokie genų variantai lemia atsparumą ligai ar kaip tik didesnį polinkį į ją, galima tiksliai matematiniais metodais apskaičiuoti, kokia tikimybė žmogui susirgti viena ar kita liga. Pagrindinis personalizuotos medicinos privalumas yra ligų ar net padidėjusios rizikos jomis sirgti nustatymas ankstyvojoje stadijoje, kartais dar iki pasireiškiant simptomams. Asmeniui pritaikyta medicina yra genetikos amžiaus išradimas, padedantis biocheminiais ir molekuliniais tyrimais nustatyti tikslią ligos prognozę, diagnozę, parinkti konkrečiai asmeniui skirtą gydymą, sekti ligos eigą ir netgi kurti naujus preparatus, idealiai pritaikytus konkrečiam asmeniui.
Asmeninės medicinos užuomazgų galima rasti ir įprastoje medicinoje – dar senovėje turtingieji turėdavo savo asmeninius gydytojus tam, kad liga ar ligos tikimybė būtų nustatyta remiantis konkretaus asmens savybėmis, o ne įprastais, bendraisiais medicinos diagnozavimo principais. Įprastais metodais diagnozuojant ligą taip pat atsižvelgiama į asmenines paciento savybes – amžių, lytį, gyvybiškai svarbių organų būklę. Taigi čia ir atsiskleidžia nuosavo genomo svarba gydant ligas. Žmogaus genomas susideda iš koduojančių ir nekoduojančių sričių. Koduojančios sudaro tik keletą procentų genomo. Tačiau nekoduojančių sričių funkcija iki šiol nėra iki galo žinoma. Nekoduojančios sritys kiekvieno žmogaus yra skirtingos, o jų sekos turinio nustatymu remiasi biologinės giminystės ir tėvystės tyrimai. Galima sakyti, kad šios nekoduojančios DNR sekos yra savotiški genetiniai „pirštų atspaudai“, kurie padaro kiekvieną žmogų išskirtiniu DNR pokyčių, vadinamų vieno nukleotido pokyčiu (VNP), pagrindu.
DNR ypatumų iššifravimas bei genomo arba DNR paso suformavimas įmanomas išanalizavus didelės žmonių populiacijos genetinius mėginius bei susiejus juos su žiniomis apie esamą tų žmonių sveikatą. Būdama pakankamai izoliuota nuo kitų šalių ir turėdama dar iš vikingų laikų išlikusių bažnytinių knygų su informacija apie ligas, nuo kurių mirė dabartinių islandų protėviai, Islandija gali gauti itin tikslius genetiškai perduodamų ligų tyrimų rezultatus.
Kaimyninėje Estijoje taip pat vykdomas genomo projektas, pagal kurį nustatoma jo DNR sekos įvairovė bei sąsajos su ligomis. Tartu universiteto Molekulinės diagnostikos centro pastangomis suplanuota ištirti arti milijono DNR pavyzdžių. Lietuvoje genomo tyrimo projektai taip pat intensyviai vykdomi. 2011 m. vadovaujant Vilniaus universiteto Žmogaus ir medicininės genetikos katedros mokslininkams, susikūrė „LITGEN“ projektas – Lietuvos populiacijos genetinė įvairovė ir sandaros kitimai, susiję su evoliucija ir dažniausiai paplitusiomis ligomis. Šio projekto pagrindinė idėja yra atlikti Lietuvos populiacijos plataus masto genominius tyrimus ir identifikuoti būdingas genomines sritis, kurios yra reikšmingos žmogaus sveikatai. Projekto strateginiai tikslai yra:
LITGEN atliko šiuolaikinius plataus masto mokslo tiriamuosius darbus, taikant aukštąsias technologijas ir didelio našumo technologines platformas, sukaupė pakankamai didelę imtį tiriamųjų asmenų, išsamiai charakterizuotų pagal klinikinį ir biocheminį fenotipą, ir šių asmenų biomedžiagų (DNR, kraujo serumo) mėginius, t. y. sukūrė Lietuvos populiacijos biobazę.
Svarbi Lietuvoje atliekamų personalizuotos medicinos tyrimų sritis yra farmakogenetiniai tyrimai. LSMU Kardiologijos instituto Molekulinės kardiologijos laboratorijoje atliekami tyrimai nustatant individualų asmens genotipą, kuris lemia ligonio reakciją į kraują skystinančius vaistus. Pagal šiuos genetinius tyrimus galima personalizuotai parinkti varfarino ar klopidogrelio dozę. Antai vienam pacientui užtenka 1/4 vidutinės vaisto paros dozės ir jam bus pakankamas kraujo krešėjimą mažinantis efektas, o kitam pacientui reikės dvigubos dozės, ir tik tada pakaks vaisto. DNR duomenų iššifravimas bei asmens genetinio paso sukūrimas klinikinei medicinai svarbus keletu aspektų:
. Sveikų asmenų genetinio polinkio į nepaveldimas ligas tikimybei nustatyti. Pagal šias tikimybes gali būti
sudaromas profilaktinių tyrimų patikrų planas, pateikiamos gyvenimo būdo rekomendacijos – pacientui gali tekti atsisakyti žalingų įpročių, keisti darbo ir poilsio laiką, papildyti maisto racioną tinkamais maisto produktais arba visai atsisakyti netinkamų.
. Sveikų asmenų genetinių mutacijų nešiojimui nustatyti, kuris svarbus jų vaikų genetinių ligų rizikos laipsnio nustatymui bei prevencijai. Tai aktualu vadinamųjų autosominiu recesyviniu arba su X chromosoma susijusių paveldimų ligų įvertinimui.
. Personalizuotai ir saugiai prenatalinei nėščiųjų patikrai.
Sveikų asmenų genetinio polinkio į ligas tikimybės nustatymas
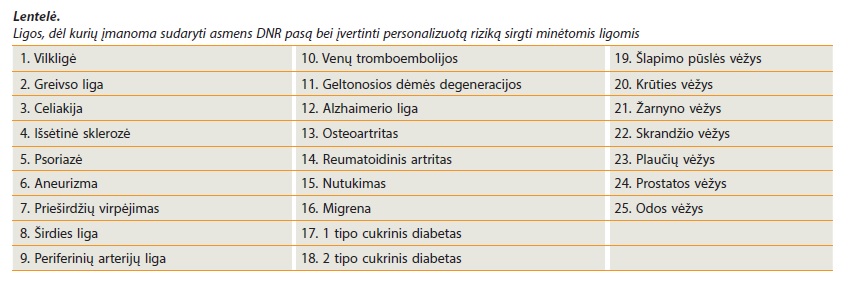
Vienas svarbiausių personalizuotos medicinos siūlomų pranašumų, kuris realia apimtimi pakeitė patį suvokimą apie ligų profilaktiką, tai – prevenciniai genetiniai tyrimai. Atliekant genetinius tyrimus galima sužinoti individualų žmogaus polinkį į ligas ir sirgti ligomis, paveldėtomis iš tolimiausių protėvių. Taigi genetinio polinkio į ligas DNR tyrimai padeda sudaryti asmens DNR paso variantą. Genetinio polinkio į ligas testas yra paremtas vieno nukleotido polimorfizmais, tam tikromis vietomis genome, susijusiomis su tiriamų ligų išsivystymu. Tyrimai atliekami dėl dažniausiai pasitaikančių ligų, kurios pateikiamos lentelėje. DNR technologija grįsti diagnostiniai tyrimai padeda sužinoti tikslią žmogaus giminės ligos istoriją (anamnezę) – kurios ligos gali būti paveldėtos ir perduotos genetiškai iš kartos į kartą, taip pat – įvertinti įvairių ligų tikimybę, esančią nepriklausomai nuo anamnezės, ir sveikatos pablogėjimo riziką sulaukus vyresnio amžiaus. Šie genetiniai tyrimai nustato įvairių ligų ar būklių riziką bet kuriam žmogui, o tai padeda užkirsti kelią ligai išsivystyti, t. y. kiekvienas žmogus iš prigimties turi vieną ar kitą silpną savo organizmo vietą, kuri, esant nepalankioms sąlygoms (netinkamam gyvenimo būdui, žalingiems įpročiams, kenksmingoms darbo sąlygoms ir kt.), gali paskatinti ligos vystymąsi. Daugeliu atvejų žmogaus genomą iššifruojantis tyrimas, nustatantis ligų tikimybes, įgalina neprarasti budrumo, laiku imtis atitinkamų profilaktikos priemonių ir neleisti ligai išsivystyti.
Sveikų asmenų genetinių mutacijų nešiojimo nustatymas
Nešiotojų patikros tyrimas yra paprastas tyrimas, kuriuo tikrinama, ar tiriamasis turi vieną ar daugiau autosominiu recesyviniu būdu paveldimų ligų ar su X chromosoma susijusių genetinių ligų. Dauguma šių ligų genų nešiotojų yra sveiki, tačiau jie taip pat gali susilaukti vaikų, sergančių genetinėmis ligomis. Testo rezultatai padeda priimti informuotą sprendimą geriau suprantant nešiotojo statuso reikšmę. Horizont tyrimą galite atlikti prieš nėštumą arba jo metu. Autosominiu recesyviniu būdu paveldimas ligas ar su X chromosoma susijusias genetines ligas lemia tam tikro geno pokytis (mutacija) viename gene ar genų poroje, kuris turi įtakos tam, jog genai ar genų pora funkcionuoja netinkamai arba visai nefunkcionuoja. Kai genų veikla nėra tinkama, kūdikiui ar vaikui gali kilti rimtų sveikatos sutrikimų.
Autosominiu recesyviniu būdu paveldimų ligų paveldimumas
Kad būsimas vaikas turėtų didelę riziką sirgti šio tipo ligomis, nešiotojais turi būti ir mama, ir tėtis. Jei abu tėvai yra tos pačios mutacijos nešiotojai, tada tikimybė kiekvieno nėštumo metu, kad kūdikis bus paveiktas šios genų mutacijos, yra 1 iš 4 arba 25 proc. Šiandien ir Lietuvoje („InMedica Alfa“) pora dar iki vaiko pradėjimo gali atlikti 274 genetinius sutrikimus lemiančių mutacijų testą bei išsiaiškinti, ar šių „asimptominių“ pokyčių neturi.
Kokie yra reprodukciniai pasirinkimai, jei asmuo yra mutacijos nešiotojas
Dėl autosominiu recesyviniu būdu paveldimų ligų jūs ir jūsų partneris turi būti tos pačios mutacijos nešiotojas, tada jūsų kūdikis turi didelę riziką sirgti paveldima liga. Jei jūs ir jūsų partneris abu esate tos pačios mutacijos nešiotojai arba jei moteris yra su X chromosoma susijusių genetinių ligų nešiotoja, galimi šie reprodukciniai sprendimai:
. natūralus pastojimas,
. nėščiųjų prenataliniai invaziniai tyrimai, tokie kaip vaisiaus vandenų tyrimas (amniocentezė) arba choriono gaurelių biopsija (CGB),
. dirbtinis apvaisinimas mėgintuvėlyje (IVF) su preimplantacine genetine diagnostika (PGD),
. donoro, kuris nėra genetinių mutacijų nešiotojas, spermos ar kiaušialąstės panaudojimas,
. įvaikinimas.
Proveržis prenatalinėje genetinėje diagnostikoje
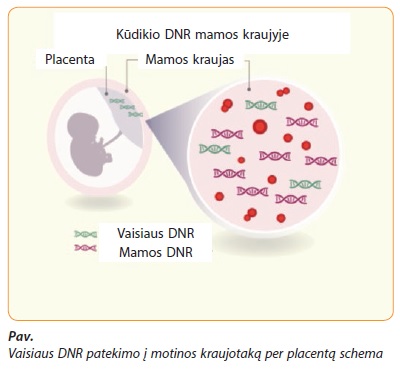
Naujausi genetikos tyrimai įrodė, kad nėščiosios kraujotakoje cirkuliuoja laisva vaisiaus DNR, kurios pėdsakus galima aptikti jau nuo 4-os nėštumo savaitės (pav.). Nuo 9-os savaitės vaisiaus DNR pasiekia koncentraciją, kuri būna pakankama atlikti tyrimui įvertinti vaisiaus chromosominėms ligoms (angl. non invasive prenatal testing – NIPT). Taikant unikalų kiekybinį VNP metodą išanalizuojamas vaisiaus ir motinos laisvos DNR rinkinys. Kiekvieno žmogaus VNP yra skirtingi, dėl to kiekvienas žmogus yra unikalus. NIPT tyrimų dėl chromosominių ligų efektyvumas yra 96–99 proc. Veiksmingiausias esti tyrimas nustatant Dauno sindromą (21 chromosomos trisomiją) (99 proc.), kiek mažiau – nustatant Edwardso (18 trisomija), Patau (13 trisomija) ir Ternerio (X monosomija) sindromus. Kai kurie šiuolaikiniai NIPT testai (Natera Panorama) įgalina nustatyti ne tik standartinius chromosomų skaičiaus pakitimus, bet ir smulkius chromosomų struktūros defektus, vadinamuosius mikrodelecinius sindromus (Angelmano, Prader-Willio, „Katės kniaukimo“, 22q11.2 (Di Džordžo) bei 1p36 delecijos ir kt.) (Natera Panorama). Šis neinvazinis testas nustato ir kūdikio lytį (100 proc. tikslumu).
Šiuolaikinis NIPT testas Natera Panorama šiandien prieinamas ir Lietuvos nėščiosioms („InMedica“ klinikos bei Motinos ir vaiko klinika). Tyrimas sudaro galimybes šalia standartinių chromosomų trisomijų bei mikrodelecinių sindromų įvertinti ir retą vaisiaus ligą – triploidiją, kada būna visų chromosomų trigubas rinkinys. Pati vaisiaus liga gali paveikti ir nėščiosios sveikatą – didinti eklampsijos riziką. NIPT tyrimų tikslumas ženkliai pagerino prenatalinių tyrimų efektyvumą. Seniau plačiai taikytų biocheminių nėščiosios tyrimų (Prisca) efektyvumas nustatant vaisiaus chromosomines ligas yra apie 80 proc., o klaidingai teigiamų rezultatų procentas yra 5–10 proc. Tai reiškia, kad iš 100 moterų 5–10-čiai tyrimai parodo padidėjusią riziką, nors iš tiesų vaikas būna sveikas. Kita vertus, tikslieji invaziniai tyrimai (amniocentezė arba choriono gaurelių biopsija) turi, kad ir labai nedidelę, komplikacijų riziką. Labai dažnai po rizikingo tyrimo dėl chromosomų trisomijų nėščiųjų biocheminio (PRISCA) rezultatų NIPT tyrimas yra tas šansas, kurį atlikus galima išvengti invazinio tyrimo poreikio bei nereikalingo streso. Todėl pasaulio genetikos ekspertai rekomenduoja NIPT kaip pirmaeilius testus besilaukiančioms moterims, kurios pageidaują tikslių ir saugių tyrimų.
Pacientės, kurios negali išnešioti kūdikio ir patiria persileidimus, taip pat turėtų būti tiriamos genetiko. Nustatyta, kad MTHFR geno mutacijos, kurių homozigotinis variantas aptinkamas apie 10 proc. populiacijos, gali sąlygoti persileidimus. Tačiau, žinant šią situaciją, pacientei, turinčiai MTHFR mutaciją, galima skirti gydymą (aktyviais folatais, vitaminais B12, B6, metioninu ir betainu), kurie keičia geno raišką ir padeda sėkmingai pastoti ir išnešioti kūdikį.
Teisė į genetinį privatumą
DNR paso įdiegimas tapo neatsiejamas nuo su tuo susijusių etinių ir teisinių klausimų. Turint DNR tyrimo duomenis apie žmogaus polinkį į tam tikras ligas, galima šią informaciją panaudoti darbo bei draudimo srityse, todėl tai gali būti genetinio diskriminavimo priežastimi. Genetinės diskriminacijos galimybė visuomenėje kelia didžiausią susirūpinimą ir baimę, kad tokia privati informacija apie asmenį gali suteikti tam tikrą poveikį draudžiantis ar bandant įsidarbinti. UNESCO Visuotinės žmogaus genomo apsaugojimo ir žmogaus teisių deklaracijos 6 straipsnyje rašoma: „Nė vienas asmuo negali būti diskriminuojamas genetinių charakteristikų, su kurių pagalba arba dėl kurių poveikio ketinama pažeisti žmogaus teises, pagrindines laisves ir žmogaus orumą, pagrindu.“
Doc. dr. Danielius Serapinas, LSMU MA Genetikos ir molekulinės medicinos klinika, Mykolo Romerio universitetas, InMedica Alfa klinikos Genetikos skyrius
Šaltinis: „Lietuvos gydytojo žurnalas“, 2016m. Nr.7



